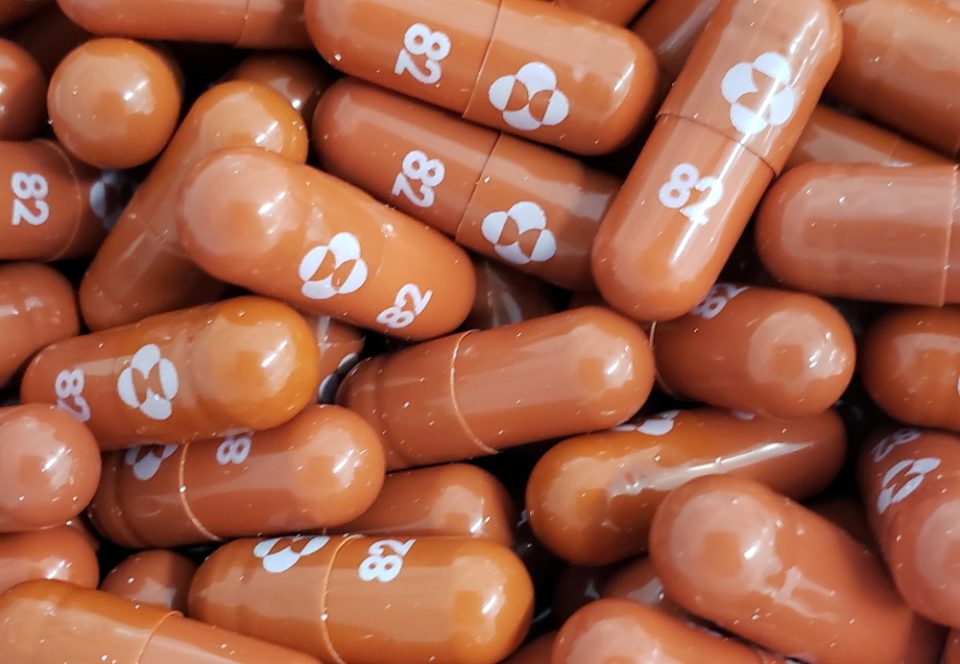
Αίτηση για χορήγηση επείγουσας άδειας για το χάπι της κατά του κορονοϊού υπέβαλε η φαρμακοβιομηχανία Merck στις αρμόδιες ρυθμιστικές αρχές των ΗΠΑ (FDA).
To χάπι έδειξε αξιόπιστα αποτελέσματα σε κλινικές δοκιμές. Το molnupiravir μείωσε τον κίνδυνο νοσηλείας ή θανάτου κατά περίπου 50% σε ασθενείς με ήπια ή μέτρια περιστατικά Covid-19, όπως ανακοινώθηκε προ ημερών. Χορηγείται από το στόμα και λειτουργεί αναστέλλοντας τον πολλαπλασιασμό του ιού στο σώμα.
Εάν εγκριθεί από τους ρυθμιστικούς φορείς, το molnupiravir θα είναι το πρώτο από του στόματος αντιιικό φάρμακο για την Covid-19.
O EMA ξεκίνησε την αξιολόγηση του χαπιού της Merck
Η Merck ανακοίνωσε την περασμένη εβδομάδα ότι, σύμφωνα με μια κλινική δοκιμή, το φάρμακό της, με την ονομασία molnupiravir, μείωσε στο μισό τους κινδύνους να νοσηλευτούν και να πεθάνουν ασθενείς με Covid-19, κάτι που θα μπορεί να αποτελέσει σημαντικό επίτευγμα στον αγώνα κατά της πανδημίας.
«Θα εξετάσουμε το ενδεχόμενο να ξεκινήσουμε μια συνεχή αξιολόγηση αυτού του σκευάσματος μέσα στις επόμενες ημέρες», δήλωσε ο επικεφαλής στρατηγικής εμβολιασμού του EΜΑ, Mάρκο Καβαλέρι.
Ο EMA γνωρίζει τα «πρώτα αποτελέσματα που κοινοποίησε η εταιρεία» Merck σχετικά με αυτό το νέο φάρμακο, πρόσθεσε ο Καβαλέρι κατά τη διάρκεια συνέντευξης Τύπου.
Αυτό το αμερικανικό εργαστήριο ανακοίνωσε την Παρασκευή ότι σχεδιάζει να υποβάλει σύντομα αίτηση στις ΗΠΑ για άδεια κυκλοφορίας του χαπιού.
Η κλινική δοκιμή της Merck και του συνεργάτη της Ridgeback Biotherapeutics πραγματοποιήθηκε σε 775 άτομα που είχαν ήπιας έως μέτριας μορφής νόσηση με την Covid-19 με τουλάχιστον έναν επιβαρυντικό παράγοντα κινδύνου.
Έλαβαν θεραπεία εντός πέντε ημερών μετά την εμφάνιση των συμπτωμάτων.
Το ποσοστό νοσηλείας ή θανάτου σε ασθενείς που έλαβαν το φάρμακο ήταν 7,3%, έναντι 14,1% εκείνων που έλαβαν εικονικό φάρμακο.
Δεν καταγράφηκαν θάνατοι σε άτομα που έλαβαν το molnupiravir, σε σύγκριση με οκτώ στη δεύτερη ομάδα.Η διαδικασία κυλιόμενης αξιολόγησης επιτρέπει στον EMA να επανεξετάσει τα δεδομένα ασφάλειας και αποτελεσματικότητας εμβολίων καθώς αυτά διατίθενται, ακόμη και πριν υποβληθεί επίσημο αίτημα για έγκριση.
Σκοπός του είναι να επιταχύνει την αξιολόγηση μιας αίτησης για άδεια κυκλοφορίας. Για την έγκριση μπορεί να χρειαστούν αρκετοί μήνες.